Otkrićem kako se atom sastoji od električno pozitivne jezgre i električno negativnih elektrona mnogi fizičari su počeli po analogija su zvijezdama i planetima smatrali kako se elektroni vrte oko jezgre kao planeti oko planeta. Daljnjim istraživanjem uvidjelo se kako to nije tako te su fizičari čestica počeli tvrditi kako atomi skaču oko jezgre po nepoznatim pravilima.
Na elektrone koji se nalaze u atomu utječu četiri sile; električno negativna i električno pozitivna sila te slaba nuklearna sila i jaka nuklearna sila.
Električno pozitivna jezgra privlači elektrone prema sebi, a električno negativni elektroni odbijaju jedni druge. Svaka jezgra može uz sebe vezati onoliko električno negativnih elektrona koliko u sebi ima električno pozitivnih protona.
Slaba i jaka nuklearna sila je malo teže razumljiva, a djelovanje ovih sila je po dosegu približno poput promjera atoma.
Električno pozitivna jezgra privlači električno negativne elektrone, a kada se oni jezgri previše približe tada nuklearne sile sprječavaju elektrone da dođu do jezgre. Ako elektron uslijed velike brzine uspije doći do jezgre tada se električno pozitivne i električno negativne čestice spajaju, čime se proton i elektron pretvaraju u energiju, što je poznato kao nuklearna reakcija.
U atomu elektron se postavlja na određenu poziciju udaljenu od jezgre kod koje su sile koje ga privlače prema jezgri i one sile koje ga odbijaju od jezgre izjednače. Ako se takvom atomu sa jednim elektronom (vodik) približi neki slobodni elektron tada će se elektron u atomu postaviti na suprotnu stranu jezgre zato što se elektroni odbijaju. Ako se tada sa druge strane pojavi neki drugi slobodni elektrona tada će se elektron u jezgri postaviti na poziciju kod koje je jednako udaljen od oba vanjska slobodna elektrona.
Kod atoma helija oko jezgre se nalaze 2 elektrona koji se međusobno odbijaju, te se stoga ova dva elektrona međusobno postavljaju na pozicije sa suprotnih strana jezgre. Ako se u blizini ovog atoma pojavi slobodni elektron tada se elektroni unutar atoma postavljaju u poziciju u kojoj su jednako udaljeni od ovog slobodnog elektrona. Na taj način dva elektrona i jezgra se uvijek nalaze na jednom pravcu.
Kod atoma sa tri elektrona elektroni se oko jezgre postavljaju u ravninu u oblik trokuta u čijoj sredini je jezgra. Ako se u blizini pojavi slobodni elektron on odbija najbliži elektron u atome, čime se istovremeno pomiču i druga dva elektrona u poziciju kod koje su sva tri elektrona jednako udaljena od vanjskog slobodnog elektrona.
Kod atoma sa 4 elektrona elektroni se postavljaju u oblik trostrane piramide kod koje su vrhovi piramide jednako udaljeni jedni od drugih. Ako se takvom atomu približi vanjski slobodni elektron tada se najbliži elektron u atomu odmiče, čime se pomiču i svi drugi elektroni, te se postavljaju u poziciju kod koje su 3 elektrona jednako udaljena od vanjskog elektrona, dok je četvrti elektron postavljen na suprotnu stranu jezgre. Pri tome elektroni i dalje zadržavaju oblik trostrane piramide.
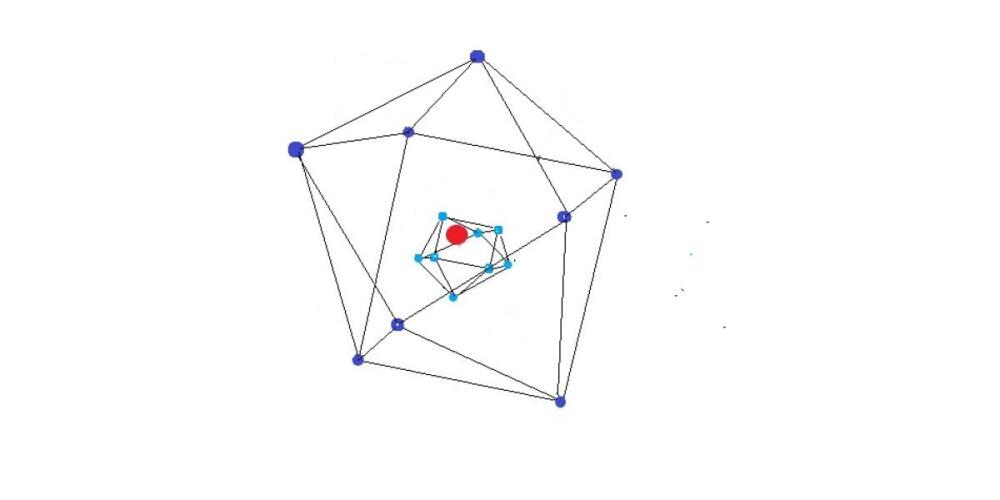
Kod atoma sa 5 elektrona u atomu oni se postavljaju u oblik tijela sa 5 vrhova koji su međusobno udaljeni jedni od drugih. Na isti način se postavljaju elektroni i kod 6 ili 7 elektrona.
Kod atoma sa 8 elektrona oni se postavljaju u oblik dva pravilna četverokuta koji su međusobno pomaknuta na stranu za 45 stupnjeva. Time se dobiva prostorni raspored elektrona koji čine vrhove tijela koje ima dva međusobno paralelna istostranična kvadrata koji su povezani sa 8 istostraničnih trokuta. Ovakav prostorni raspored elektrona je vrlo stabilan, a prostorno tijelo koje čine elektroni izgleda kao u stranu usukana kocka.
Kod atoma sa 9 elektrona taj deveti elektron nema snage da se postavi na jednaku udaljenost od jezgre, te se on postavlja na veću udaljenost od jezgre, pri čemu je jednako udaljen od 4 najbliža elektrona pozicioniranih na nižoj udaljenosti. Svaki slijedeći elektron se postavlja na istoj udaljenosti od jezgre atoma, s tim što su jednako udaljeni jedni od drugih i od elektrona koji se nalaze na nižoj poziciji.
Kod atoma koji imaju 16 elektrona oni se postavljaju u oblik dvije usukane kocke jedne unutar druge, kao i kod atoma sa 8 elektrona. Ako se takvom atomu približi strani slobodni elektron on odbija najbliži elektron čime se pomiči u svi ostali elektroni kako bi zadržali oblik usukane kocke unutra usukane kocke.
Kod svakog slijedećeg elektrona oni se postavljaju u novu poziciju veće udaljenosti od jezgre. Koliko god se broj elektrona povećava stvara se novi sloj elektrona koji formiraju oblik kocke unutar kocke. Pri tome unutrašnji slojevi uvijek imaju oblik kocke, dok se najgornji sloj formira u prostorni oblik kod kojeg su elektroni tog sloja jednako udaljeni jedni od drugih i jednako udaljeni od od jezgre atoma.
Više u knjizi Svjetlost - čestični niz.
https://www.scribd.com/document/737625418/Svjetlost-%C4%8Desti%C4%8Dni-niz-drugo-izdanje
Oznake
Izdvojeni tekstovi